Лаборатория молекулярного моделирования и синтеза биологически активных соединений
Публикаций
150
Цитирований
2 727
Индекс Хирша
31
Необходимо авторизоваться.

Исследования ведутся в области синтеза азагетероциклических соединений, химии фтора, молекулярного моделирования для поиска биологически активных соединений, квантово-химических расчетов, разработки материалов медицинского назначения.
- Квантово-химические расчеты (Quantum chemical calculations)
- Молекулярный докинг
- Оценка цитотоксической активности (МТТ-тест, Cell-TitreGlo, резазурин, Cell/Death набор)
- Смешение полимеров
- Тонкий органический синтез
- Исследование фармакокинетики (ADMET)
Андрей Хлебников
Заведующий
Надежда Даниленко
Старший преподаватель
Елизавета Самородова
Аспирант
Александр Уваров
Аспирант
Всего публикаций
153
Всего цитирований
2739
Цитирований на публикацию
17.9
Среднее число публикаций в год
3.92
Годы публикаций
1986-2024 (39 лет)
h-index
31
i10-index
76
m-index
0.79
o-index
63
g-index
45
w-index
6
Описание метрик
h-index
Учёный имеет индекс h, если h из его N статей цитируются как минимум h раз каждая, в то время как оставшиеся (N - h) статей цитируются не более чем h раз каждая.
i10-index
Число статей автора, получивших не менее 10 ссылок каждая.
m-index
m-индекс ученого численно равен отношению его h-индекса к количеству лет, прошедших с момента первой публикации.
o-index
Среднее геометрическое h-индекса и числа цитирований наиболее цитируемой статьи ученого.
g-index
Для данного множества статей, отсортированного в порядке убывания количества цитирований, которые получили эти статьи, g-индекс это наибольшее число, такое что g самых цитируемых статей получили (суммарно) не менее g2 цитирований.
w-index
Если w статей ученого имеют не менее 10w цитирований каждая и другие статьи меньше, чем 10(w+1) цитирований, то w-индекс исследователя равен w.
Топ-100
Области наук
Журналы
Цитирующие журналы
Цитируемые журналы
Издатели
|
5
10
15
20
25
30
35
40
|
|
|
MDPI
40 публикаций, 26.14%
|
|
|
Elsevier
29 публикаций, 18.95%
|
|
|
Springer Nature
28 публикаций, 18.3%
|
|
|
Pleiades Publishing
13 публикаций, 8.5%
|
|
|
Wiley
9 публикаций, 5.88%
|
|
|
American Chemical Society (ACS)
6 публикаций, 3.92%
|
|
|
American Society for Pharmacology and Experimental Therapeutics
6 публикаций, 3.92%
|
|
|
Taylor & Francis
4 публикации, 2.61%
|
|
|
Frontiers Media S.A.
4 публикации, 2.61%
|
|
|
Hindawi Limited
2 публикации, 1.31%
|
|
|
Bentham Science Publishers Ltd.
1 публикация, 0.65%
|
|
|
Royal Society of Chemistry (RSC)
1 публикация, 0.65%
|
|
|
Mary Ann Liebert
1 публикация, 0.65%
|
|
|
Ivanovo State University of Chemistry and Technology
1 публикация, 0.65%
|
|
|
Institute of New Chemical Technologies and Materials of Al-Farabi Kazakh State National University
1 публикация, 0.65%
|
|
|
Beilstein-Institut
1 публикация, 0.65%
|
|
|
Arterialnaya Gipertenziya
1 публикация, 0.65%
|
|
|
The American Association of Immunologists
1 публикация, 0.65%
|
|
|
Institute of Biochemistry
1 публикация, 0.65%
|
|
|
5
10
15
20
25
30
35
40
|
Организации из публикаций
Страны из публикаций
|
20
40
60
80
100
120
140
160
|
|
|
Россия
|
Россия, 143, 93.46%
Россия
143 публикации, 93.46%
|
|
США
|
США, 79, 51.63%
США
79 публикаций, 51.63%
|
|
Италия
|
Италия, 22, 14.38%
Италия
22 публикации, 14.38%
|
|
Казахстан
|
Казахстан, 12, 7.84%
Казахстан
12 публикаций, 7.84%
|
|
Турция
|
Турция, 11, 7.19%
Турция
11 публикаций, 7.19%
|
|
Страна не определена
|
Страна не определена, 10, 6.54%
Страна не определена
10 публикаций, 6.54%
|
|
Великобритания
|
Великобритания, 6, 3.92%
Великобритания
6 публикаций, 3.92%
|
|
Украина
|
Украина, 5, 3.27%
Украина
5 публикаций, 3.27%
|
|
Республика Корея
|
Республика Корея, 3, 1.96%
Республика Корея
3 публикации, 1.96%
|
|
Китай
|
Китай, 2, 1.31%
Китай
2 публикации, 1.31%
|
|
Бельгия
|
Бельгия, 2, 1.31%
Бельгия
2 публикации, 1.31%
|
|
Кипр
|
Кипр, 2, 1.31%
Кипр
2 публикации, 1.31%
|
|
Швеция
|
Швеция, 2, 1.31%
Швеция
2 публикации, 1.31%
|
|
Испания
|
Испания, 1, 0.65%
Испания
1 публикация, 0.65%
|
|
СССР
|
СССР, 1, 0.65%
СССР
1 публикация, 0.65%
|
|
20
40
60
80
100
120
140
160
|
Цитирующие организации
Цитирующие страны
- Мы не учитываем публикации, у которых нет DOI.
- Статистика пересчитывается раз в сутки.
Направления исследований
Разработка новых фторуглеродных аза-гетероциклов в качестве противоопухолевых агентов и средств их адресной доставки
+
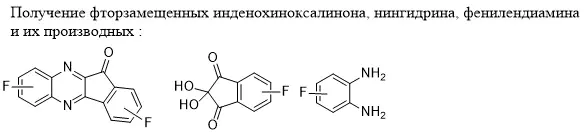
Разработка фундаментальных основ для создания и внедрения новых эффективных противоопухолевых препаратов позволяет уменьшить бремя социально значимых онкологических заболеваний. В настоящее время разработка новых эффективных лекарственных препаратов часто затрудняется низкой биодоступностью, избирательностью противоопухолевого действия получаемых биологически активных соединений, оказывающих впоследствии нежелательные побочные эффекты. Отдельную проблему представляет разработка материалов как системы адресной доставки и восстановления дефектов, возникающих после удаления опухоли с частичной резекцией ткани. Такие материалы должны обладать противоопухолевой активностью, при этом способствовать регенерации тканей и не вызывать избыточных иммунных реакций, таких как воспаление и отторжение. С точки зрения разработки средств адресной доставки – применение материалов, подвергающихся слишком длительной деградации, снижает эффективность лекарственной терапии, так как снижается скорость и объем поступления лекарственного средства в ткань или системный кровоток. Проект направлен на решение проблемы увеличения продолжительности жизни онкологических больных с помощью создания новых эффективных противоопухолевых препаратов с улучшенной биодоступностью и селективностью и материалов на их основе для таргетной терапии. Проект представляет собой комплексное междисциплинарное исследование, включающее молекулярное конструирование, синтез на основе химических модификаций оригинальных гибридных структур, имеющих в своем составе фармакафорные группировки, оценку спектра биологической активности новых соединений, метод электроспиннинга для получения материалов на основе биоразлагаемых полимеров с включением биологически активного вещества. В качестве базовых фармакофоров для создания гибридных структур, будут использованы производные нингидрина (2,2-дигидроксииндан-1,3-диона) и инденохиноксалина, обладающие противораковой активностью. В проекте будет использована концепция замены связи C-H на связь C-F путем органического синтеза, поскольку замещение атомов водорода бензольных (и иных ароматических) фрагментов атомами фтора часто модифицирует физико-химические, биологические, в том числе фармацевтические свойства. В основу программы химических модификаций будут также положены результаты молекулярного моделирования взаимодействия гибридных структур с активными сайтами широкого ряда раковых биомишеней, создание библиотек планируемых к синтезу соединений и их виртуальный скрининг. Будет проведена оценка профиля ADMET полученных соединений как характеристики их биодоступности и безопасности. Для оценки безопасности также будет определена цитотоксичность перспективных соединений по результатам скрининга на культуре клеток. Оптимизация соединений с точки зрения спектра их биологической активности и безопасности будет проводиться с применением методов компьютерного моделирования, в том числе мультитаргетного анализа связи структура – активность (SAR и QSAR модели). Научная новизна исследования заключается в получении оригинального класса органических соединений на основе фторсодержащих инденохиноксалинов и нингидринов и исследовании различных параметров их биодоступности, растворимости и безопасности с применением направленного органического синтеза, молекулярного моделирования и квантово-химических расчетов. Наиболее перспективные агенты будут впервые включены в состав биодеградируемых материалов, и исследована динамика высвобождения этих соединений из их объема. Будут изучены физико-химические свойства полученных материалов и сделан вывод о возможности их дальнейшего использования в антирецидивной терапии после удаления опухолей и доставки фторуглеродных аза-гетероциклов. Результаты данного проекта станут фундаментальной основой для развития новых подходов к лечению онкологических заболеваний и шагом к персонализированной медицине. (Грант РНФ №24-73-00202).
SuFEx реакции в получении новых производных бензоксазола – создание новых противораковых препаратов и средств их доставки
+
Лечение онкологических заболеваний является весьма актуальной задачей. После удаления опухоли возникают различные проблемы, в том числе образование полости, на месте которой впоследствии образуется рубцовая ткань, а также оставшиеся раковые клетки, которые могут снова спровоцировать рост опухоли. Решением этих проблем может стать биоразлагаемый материал, наполненный цитотоксическим препаратом, который в конечном итоге будет заменен нативной тканью. Для достижения высокой интеграции идеальный материал должен точно имитировать морфологию восстанавливаемых тканей. Материалом, который может быть использован для этой цели, являются волокнистые скаффолды, изготовленные из биоразлагаемого полимера методом электроспиннинга и заполненные цитотоксическим лекарственным средством. Бензоксазол - один из важнейших гетероциклов, который был обнаружен во многих биологически активных соединениях. Производные бензоксазола обладают широким разнообразием биологической активности, включая противоопухолевое, противомикробное, противовирусное, антигистаминное, антиоксидантное, противоязвенное, противосудорожное, глистогонное, антидепрессивное и обезболивающее действие. Некоторые важные природные соединения, такие как кальцимицин, накиджинол и боксазомицин А, содержат в своей структуре бензоксазольный фрагмент. Многочисленные производные бензоксазола описаны как агонисты или антагонисты важных рецепторов. Среди синтетических и встречающихся в природе производных бензоксазола есть соединения, проявляющие цитотоксическую активность против нескольких линий раковых клеток человека. Клик-реакции серофторидного обмена (VI) (sulfur fluoride exchange - SuFEx) успешно используются для синтеза малых молекул, в химической биологии для мечения белков, в материаловедении для получения полимерных материалов и модификации поверхности. Несмотря на это, реакции SuFEx не получили широкого распространения для получения производных бензоксазола. Таким образом, актуальной задачей является получение производных бензоксазола с использованием SuFEx реакций, что позволит разработать новые биологически активные соединения для противораковой терапии. Такие соединения можно использовать как модельные противораковые препараты для загрузки в волокнистые скаффолды, так как, помимо биологической активности, многие бензоксазолы проявляют флуоресцентные свойства, что делает более удобным изучение полученных материалов. (Грант РНФ № 23-23-00460)
Разработка киназных ингибиторов MKK7/JNK в качестве противоопухолевых агентов
+
Онкологические заболевания являются серьезной клинической проблемой. Разработка фундаментальных основ для создания и внедрения новых эффективных противоопухолевых препаратов позволит уменьшить бремя социально значимых онкологических заболеваний на уровне общества, семьи и отдельного пациента. Исследования в области биомедицинской науки последних лет позволили открыть новые молекулярные мишени для лечения онкологических заболеваний. Важными молекулярными мишенями для контроля пролиферации опухолевых клеток являются митоген- активируемая киназа киназы 7 (MKK7) и c-Jun N-терминальная киназа (JNK) (Tominaga et al., 2010; Park et al., 2019; Abdelrahman et al., 2021; Dougherty et al., 2022). MKK7 фосфорилирует JNK, играя роль прямого активатора этой киназы (Davis, 2000). Одними из немногих известных к настоящему времени синтетических ингибиторов MKK7 является нафтохинон NSC95397 (2,3-бис[(2-гидроксиэтил)тио]-1,4-нафтохинон) и его аналоги (Yang et al., 2014; Schepetkin et al., 2019). С другой стороны, введение в структуру ингибиторов киназ оксимной группировки значительно повышает их ингибирующую активность в отношении ряда протеинкиназ, что сопровождается усилением противоопухолевых свойств этих агентов (Lu et al., 2016; Schepetkin et al., 2021). Разработка новых ингибиторов киназ является одним из перспективных направлений в фармакологии для терапии многофакторных заболеваний, включая опухоли различного генеза (Bansal and Silakari, 2014). Создание и изучение биологических эффектов новых соединений на основе киназных ингибиторов MKK7/JNK позволит внести существенный вклад в решение проблемы лечения ряда онкологических заболеваний. (Грант РНФ № 25-15-00334)
Публикации и патенты
Найдено
Ничего не найдено, попробуйте изменить настройки фильтра.
Марк Борисович Плотников, Вера Ивановна Смольякова, Галина Анатольевна Чернышева, Олег Ибрагимович Алиев, Анна Марковна Анищенко, Анастасия Витальевна Сидехменова, Игорь Александрович Щепеткин, Дмитрий Николаевич Аточин, Андрей Иванович Хлебников
RU2791639C2,
2020
Марк Борисович Плотников, Олег Ибрагимович Алиев, Анна Марковна Анищенко, Анастасия Витальевна Сидехменова, Игорь Александрович Щепеткин, Дмитрий Николаевич Аточин, Андрей Иванович Хлебников
RU2740379C1,
2021
Ольга Александровна Кайдаш, Андрей Иванович Хлебников, Игорь Александрович Щепёткин, Владимир Владимирович Иванов, Анастасия Руслановна Коврижина, Евгений Евгеньевич Буйко, Екатерина Александровна Перина
RU2732503C1,
2020
Марк Борисович Плотников, Вера Ивановна Смольякова, Галина Анатольевна Чернышева, Игорь Александрович Щепеткин, Дмитрий Николаевич Аточин, Андрей Иванович Хлебников
RU2696583C1,
2019
Игорь Александрович Щепеткин, Дмитрий Николаевич Аточин, Андрей Иванович Хлебников, Марк Борисович Плотников, Галина Анатольевна Чернышева, Вера Ивановна Смольякова
RU2680526C1,
2018
2024
—
2026
| Коврижина Анастасия Руслановна
2024
—
2026
| Хлебников Андрей Иванович
2023
—
2024
| Даниленко Надежда Викторовна
Партнёры
Адрес лаборатории
Томск, пр-т Ленина 2, строение 33, помещение 202
Необходимо авторизоваться.