Раскрыты универсальные механизмы долгожительства у млекопитающих
Продолжительность жизни сильно отличается у разных видов млекопитающих и обычно растет с увеличением массы тела животного. Так, крошечная землеройка живет немногим больше 3 лет, тогда как гренландский кит может разменять не одну сотню лет. Вместе с тем, есть и исключения из правила. Например долгожительством, но не размерами, отличаются голый землекоп, некоторые летучие мыши и человек, что обусловлено эволюционным изменением генов и, соответственно, множества метаболических путей.
Продолжительность жизни млекопитающих может быть увеличена и внутри вида. Исследования на животных показывают, что на нее влияют генетические, фармакологические и экологические факторы, такие как нокаут гена рецептора гормона роста GHR, применение иммунодепрессанта рапамицина, ограничение калорий и прочие. Однако все еще необходимо до конца не ясны универсальные молекулярные механизмы долголетия, а также их причинно-следственная связь со старением. Раскрыв их, можно не только продлить жизнь человека, но и улучшить состояние его здоровья в пожилом возрасте.
Международная группа, в которую вошли исследователи Института физико-химической биологии имени А.Н. Белозерского Московского государственного университета, провела секвенирование РНК и охарактеризовала активность генов из 6 типов тканей (мозг, почки, печень, мозжечок, сердце и семенники) млекопитающих 41 вида, включая рекордсменов-долгожителей. С помощью метаанализа авторы смогли определить видо- и тканеспецифичные, а также универсальные биомаркеры, связанные со старением.
Транскриптомные изменения, связанные с возрастом у млекопитающих, в целом оказались сходны в различных органах и у разных видов. Многие из них были связаны с уже установленными признаками старения, включая нарушение работы митохондрий, утрачивание способности клеток к делению и воспаление. Активность связанных с этими процессами генов также положительно коррелировала с продолжительностью жизни, однако их влияние отличалось у разных видов. Например препарат-ингибитор комплекса NF-kB (транскрипционный фактор, играющий важную роль в клеточной гибели, иммунном ответе и клеточном цикле) улучшал выживание фибробластов короткоживущих животных в условиях окислительного стресса, но был значительно менее эффективен в клетках долгоживущих.
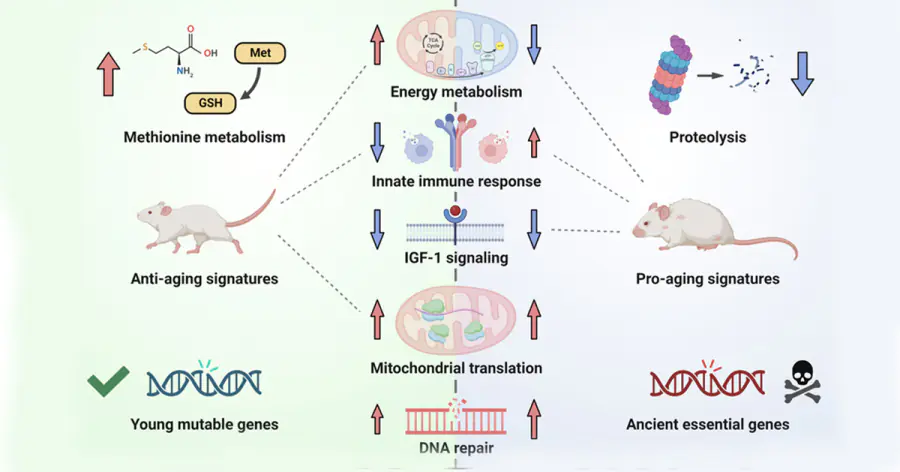
Маркеры долголетия, согласно исследованию, связаны с механизмами, противостоящими возрастным изменениям. Например, чтобы избежать накопления дефектных белков, которые могут неправильно работать и ухудшать состояние организма, у видов-долгожителей усилен синтез (а значит, и сменяемость) белков митохондрий — энергостанций клетки.
Также авторы обнаружили интересную связь между долголетием и эволюционным возрастом генов. Оказалось, что биомаркеры долгоживущих видов чаще представляют собой более древние и консервативные гены, чьи мутации достаточно критичны для работы организма. В то же время генетические изменения, которые в экспериментах показали способность отсрочить смерть от старости и в целом улучшали состояние пожилых животных, обычно затрагивали более молодые гены, устойчивые к мутациям и вариации числа копий.
Исследователи пришли к выводу, что наилучшей стратегией по увеличению продолжительности жизни — что мыши, что человека — будет сочетание тонкой настройки фундаментальных механизмов (например, регуляция восстановления ДНК и активности иммунитета) и изменение относительно молодых метаболических путей (например, окислительного фосфорилирования, необходимого для получения энергии). На основе этого они предложили несколько вариантов возможных генетических модификаций — пока только мышей. Авторы надеются, что их исследование и новые эксперименты помогут в борьбе со старением и связанными с ним болезнями.
