Лаборатория функциональных полимеров и полимерных материалов
Работа нашей лаборатории направлена на изучение закономерностей взаимодействия полимеров с клетками и создание новых полимерных систем, способных избирательно подавлять рост раковых клеток.
В последние 6-7 лет основное внимание уделяется полимерным системам, способным генерировать синглетный кислотрод в результате реакции с биогенной перекисью водорода, продуцируемой раковыми клетками. Разработаны полимерные системы, способные излучать свет и генерировать синглетный кислород при контакте с раковыми клетками, продуцирующими повышенные количесива пероксида водорода.
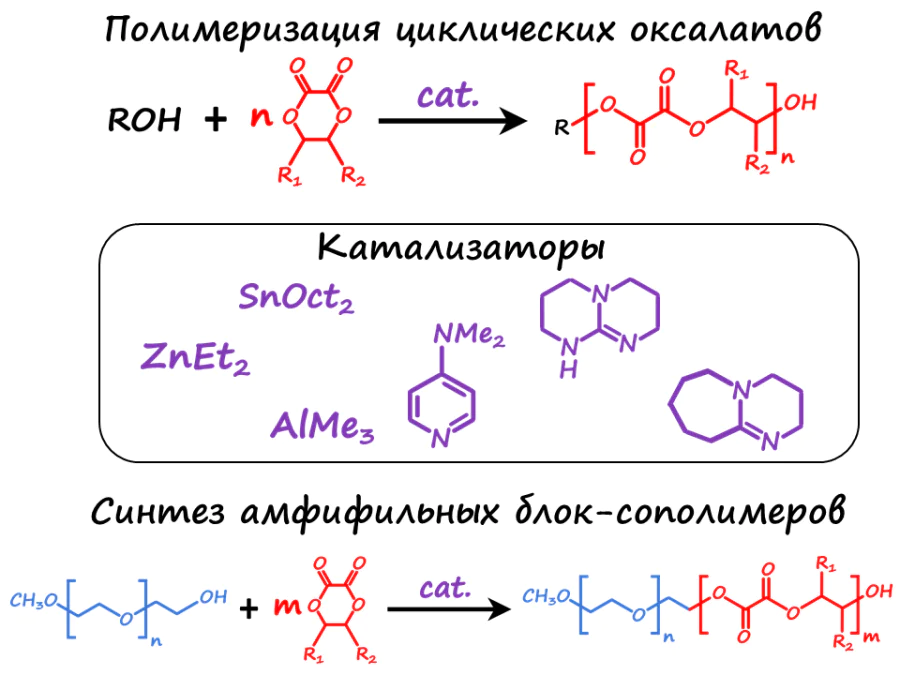
Данные полимерные системы состоят из трех основных компонентов: ароматических эфиров щавелевой кислоты (оксалатов), фотосенсибилозатора, в качестве которго может выступать порфирин и ряд других органических и металлоорганических соединений, и амфифильный сополимер, позволяющий получить устойчивую коллоидную систему из нерастворимых в воде компонентов и защитить эти компоненты от разрушаюшего действия воды.
Важнейшим условием применимости таких систем в противоопухолевой терапии является их биосовместимость. Поэтому в нашей лаборатории ведутся исследования по синтезу биодеградируемых амфифильных сополимеров, имеющих высокое сродство к компонетам хемилюминесентной системы.
- Флуоресцентная Спектроскопия
- Колоночная хроматография
- Тонкослойная хроматография
- Высоко-эффективная жидкостная хроматография (ВЭЖХ)
- Культура клеток и тканей
- Флуоресцентная микроскопия
- Просвечивающая микроскопия высокого разрешения
- Полимеризация с раскрытие цикла
- Хемилюминесценция
- Химически индуцированная фотодинамическая терапия
- Динамическое светорассеяние
Топ-100
Области наук
Журналы
Цитирующие журналы
Издатели
|
5
10
15
20
25
|
|
|
Elsevier
22 публикации, 23.66%
|
|
|
Pleiades Publishing
21 публикация, 22.58%
|
|
|
Wiley
15 публикаций, 16.13%
|
|
|
American Chemical Society (ACS)
10 публикаций, 10.75%
|
|
|
Springer Nature
7 публикаций, 7.53%
|
|
|
OOO Zhurnal "Mendeleevskie Soobshcheniya"
5 публикаций, 5.38%
|
|
|
IOP Publishing
3 публикации, 3.23%
|
|
|
Taylor & Francis
2 публикации, 2.15%
|
|
|
Royal Society of Chemistry (RSC)
2 публикации, 2.15%
|
|
|
De Gruyter Brill
1 публикация, 1.08%
|
|
|
American Physiological Society
1 публикация, 1.08%
|
|
|
MDPI
1 публикация, 1.08%
|
|
|
Akademizdatcenter Nauka
1 публикация, 1.08%
|
|
|
Institute of Biochemistry
1 публикация, 1.08%
|
|
|
5
10
15
20
25
|
Организации из публикаций
Страны из публикаций
|
10
20
30
40
50
60
70
80
|
|
|
Россия
|
Россия, 77, 82.8%
Россия
77 публикаций, 82.8%
|
|
Страна не определена
|
Страна не определена, 12, 12.9%
Страна не определена
12 публикаций, 12.9%
|
|
США
|
США, 8, 8.6%
США
8 публикаций, 8.6%
|
|
Литва
|
Литва, 6, 6.45%
Литва
6 публикаций, 6.45%
|
|
Германия
|
Германия, 5, 5.38%
Германия
5 публикаций, 5.38%
|
|
Чехия
|
Чехия, 5, 5.38%
Чехия
5 публикаций, 5.38%
|
|
СССР
|
СССР, 4, 4.3%
СССР
4 публикации, 4.3%
|
|
Чехословакия
|
Чехословакия, 4, 4.3%
Чехословакия
4 публикации, 4.3%
|
|
Грузия
|
Грузия, 3, 3.23%
Грузия
3 публикации, 3.23%
|
|
Австрия
|
Австрия, 2, 2.15%
Австрия
2 публикации, 2.15%
|
|
Австралия
|
Австралия, 1, 1.08%
Австралия
1 публикация, 1.08%
|
|
Великобритания
|
Великобритания, 1, 1.08%
Великобритания
1 публикация, 1.08%
|
|
Дания
|
Дания, 1, 1.08%
Дания
1 публикация, 1.08%
|
|
Канада
|
Канада, 1, 1.08%
Канада
1 публикация, 1.08%
|
|
Польша
|
Польша, 1, 1.08%
Польша
1 публикация, 1.08%
|
|
Саудовская Аравия
|
Саудовская Аравия, 1, 1.08%
Саудовская Аравия
1 публикация, 1.08%
|
|
10
20
30
40
50
60
70
80
|
Цитирующие организации
Цитирующие страны
- Мы не учитываем публикации, у которых нет DOI.
- Статистика пересчитывается раз в сутки.
Направления исследований
Химически-индуцированная фотодинамическая терапия
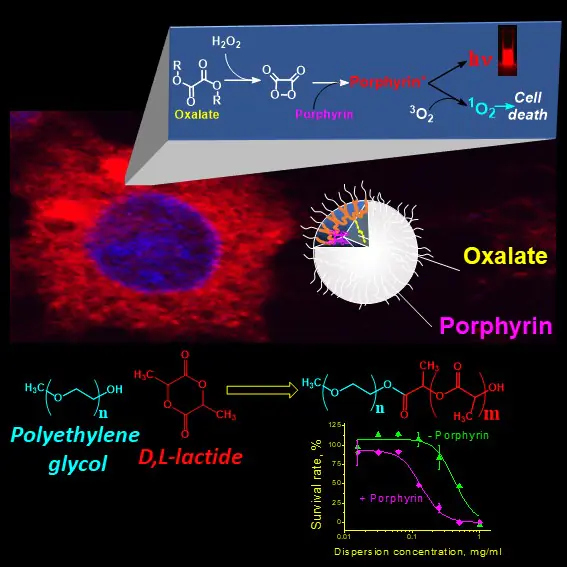
Синтез биоразлагаемых полимеров и амфифильных блок-сополимеров путем полимеризации циклических оксалатов