Эффект Доплера поможет быстро определять эффект электротерапии аритмий сердца
Российские ученые совместно с бельгийскими коллегами обнаружили, что электрические волны возбуждения клеток миокарда (мышечной ткани сердца) подчиняются эффекту Доплера, который ранее наблюдали во множестве других сред на волнах иной природы. Это поможет предсказывать направление дрейфа аномальных волн в сердце и эффективнее купировать их при помощи низковольтной терапии — щадящего метода лечения серьезных аритмий. Исследование выполнено при поддержке гранта Российского научного фонда (РНФ) и опубликовано в журнале Chaos, Solitons and Fractals.
Любые отклонения сердечного ритма от нормального синусового называются аритмией. Чаще всего человек даже не подозревает об их наличии, однако есть и более тяжелые формы. Так, некоторые опасные аритмии сердца связаны с появлением в миокарде особых волн электрического возбуждения клеток — спиральных волн, распространяющихся от точки возникновения по спирали. Они возникают либо в предсердиях, либо в желудочках. В первом случае человек их может даже не ощущать, но они повышают риск смерти от тромбов, образующихся в сердце. Во втором случае больной падает в обморок или умирает, потому что сердце начинает очень плохо перекачивать кровь.
Есть три основных подхода к лечению аритмий: прижигание проблемного участка (он погибнет и не сможет запускать патологическое возбуждение), прием специальных препаратов и электротерапия. Последний набирает все большую популярность, поскольку не такой травмирующий, как первый, и намного эффективнее второго. Суть подхода заключается в том, что кардиостимулятор имплантируют под кожу на груди пациента, а отходящие от него электроды проводят по сосудам в сердце и размещают их концы в миокарде. Прибор реагирует на аномалии сердечного ритма и пускает электрический разряд. Он может быть слабым или достаточно сильным — шоковым. Для пациента в сознании важно обеспечить безболезненность такого импульса, а потому необходимо развивать низковольтную электротерапию — пока недостаточно действенную.
«Сейчас обычно используют стимуляцию с фиксированным периодом — 80% от периода спиральной волны, но этот метод имеет эффективность лишь около 70%. Наши расчеты показывают, что целесообразно подавать импульсы с периодами от 70% до 95% от периода спиральной волны. Мы предлагаем метод, который позволит быстро определять, результативна ли стимуляция. Он основан на эффекте Доплера — изменении характеристик волны в зависимости от того, где находится наблюдатель или измеряющий прибор», — говорит руководитель проекта по гранту РНФ Сергей Правдин, кандидат физико-математических наук, ведущий научный сотрудник и заведующий сектором математического моделирования в кардиологии Института математики и механики имени Н. Н. Красовского УрО РАН.
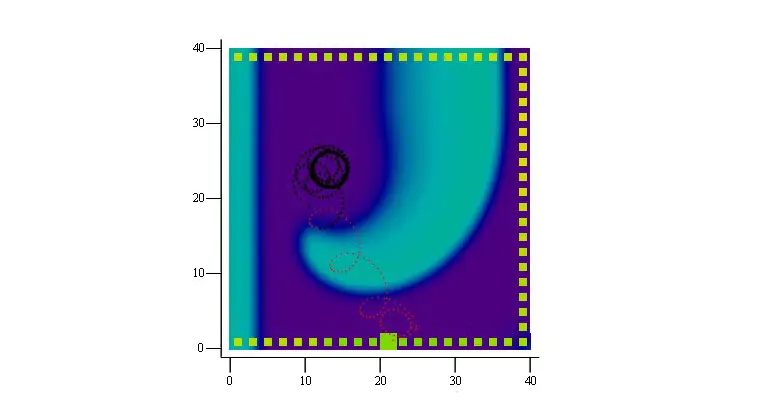
Ученые из Института математики и механики УрО РАН и Гентского университета (Бельгия) при помощи компьютерного моделирования выяснили, как в миокарде распространяются спиральные волны. Сначала они создавали стабильно вращающуюся волну, которая возникает при аритмии, а затем заставляли ее дрейфовать по компьютерному сердцу с помощью виртуальной стимуляции с электрода.
Оказалось, что период (время совершения полного колебания) дрейфующей волны зависит от места его измерения, причем достаточно точно работает формула Доплера, связывающая период волны и скорость ее дрейфа. Если измерять периоды во множестве точек, то можно предсказать наличие дрейфа волны и его направление — именно это и удалось исследователям в экспериментах с трехмерной моделью желудочка сердца, причем достаточно было всего двух-трех оборотов волны. Также авторы научились по периоду колебаний электрического потенциала клеток предсказывать скорость дрейфа.
«По результатам исследования мы вывели простые критерии эффективности стимуляции. Они охватывают и такие диагнозы, как желудочковая тахикардия, при которой очаги возбуждения находятся в желудочках и ускоряют сердцебиение. В этом случае может произойти неожиданная остановка сердца, и кардиостимулятор обычно выполняет роль дефибриллятора, подающего высоковольтный импульс. Наша цель — разработать алгоритмы, которые позволили бы обойтись без такой шоковой терапии», — отметил Сергей Правдин.