Новые препараты не дали возбудителю туберкулеза избавиться от антибиотиков
Российские ученые совместно с коллегами из ЮАР предложили препараты, которые блокируют белки-насосы бактерий, способные буквально выбрасывать лекарство из клетки. Хотя сами эти вещества не являются антибиотиками, они помогут победить лекарственную устойчивость патогенных микроорганизмов. Новые исследования раскрывают механизмы развития резистентности бактерий к антибиотикам и вносят значительный вклад в создание препаратов против штаммов туберкулеза с лекарственной устойчивостью. Работы выполнены при финансовой поддержке Российского научного фонда (РНФ). Результаты опубликованы в журнале Biomedicines.
Туберкулез стал настоящим бедствием ХХ столетия. Это инфекционное заболевание, возбудителем которого является палочка Коха, поражающая легкие человека. Успехи современной медицины позволяют выявлять и эффективно лечить туберкулез на ранних стадиях, тогда как раньше болезнь считалась непобедимой. Тем не менее, за период с 2015 по 2020 год число случаев смерти от туберкулеза во всем мире снизилось всего лишь на 9,2%. В результате пандемии COVID-19 показатели смертности также возросли, так как ухудшился доступ к лечению и профилактической терапии туберкулеза, особенно в период самоизоляции. Усугубляющим фактором стало и то, что бесконтрольный прием антибиотиков способствовал высокому уровню заболеваемости патогеном с множественной лекарственной устойчивостью.
«Одним из биохимических механизмов, обеспечивающих развитие антибиотикорезистентности, является выведение лекарства из бактериальной клетки. Отвечают за это специфические мембранные белки-насосы или эффлюксные помпы, буквально выбрасывающие опасные для возбудителя болезни молекулы. Они могут стать мишенью для эффективной борьбы с лекарственной устойчивостью», — отмечает руководитель проекта по гранту РНФ Дмитрий Маслов, кандидат биологических наук, старший научный сотрудник лаборатории генетики микроорганизмов Института общей генетики имени Н. И. Вавилова РАН.
В своей новой работе ученые из ИОГен РАН (Москва), Университета Западной Капской провинции (Южная Африка), Российского университета дружбы народов (Москва) и Южно-уральского государственного университета (Челябинск) и исследовали белковые помпы непатогенной микобактерии Mycobacterium smegmatis — близкого родственника возбудителей туберкулеза.
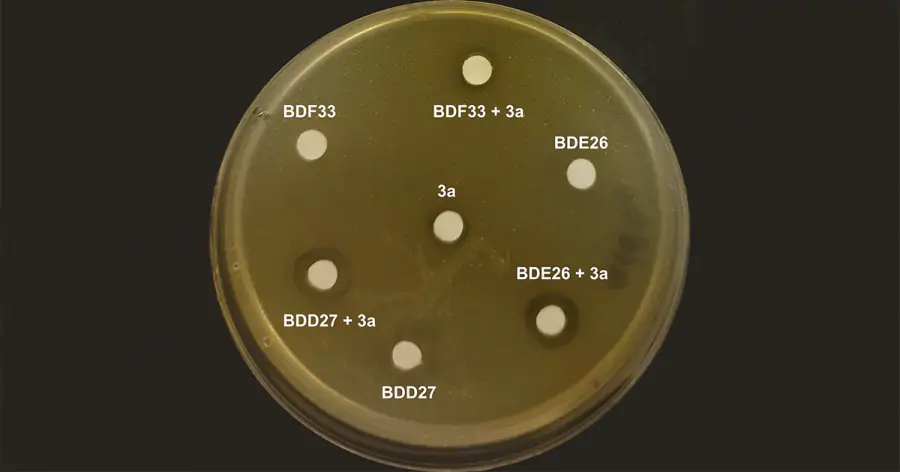
Система эффлюкса MmpS5-MmpL5 этого микроорганизма способна откачивать основные противотуберкулезные препараты. Методами молекулярного моделирования ученые создали ее теоретическую модель и определили подходящие для ее блокирования препараты из базы антибактериальных соединений ASINEX в почти 6 000 молекул. Из 100 определенных ингибиторов были отобраны пять наилучших, которые потенциально могут хорошо выводиться из организма, а также безопасны для животных клеток. Серия экспериментов in vitro на микобактериях подтвердила эффективность двух соединений, предсказанную теоретической 3D-моделью и вычислительными расчетами.
«Мы рассчитываем, что на основе полученных результатов можно будет усовершенствовать созданную модель и отобрать больше таких молекул из баз данных Gold & Platinum ASINEX. В дальнейшем их предстоит проверить непосредственно на микобактериях туберкулеза. Результаты наших исследований найдут применение в разработке новых эффективных препаратов, способных помогать существующим противотуберкулезным лекарствам, например бедаквилину, преодолевать лекарственную устойчивость туберкулеза, обусловленную эффлюксом», — подводит итог Дмитрий Маслов.

