Химики показали, как повысить избирательность энантиомерных сенсоров
Российские ученые выяснили, как можно увеличить селективность сенсоров для определения зеркальных форм (энантиомеров) биологически активных веществ, одна из которых может и не обладать необходимым эффектом. Оказалось, что избирательность специальных модификаторов, наносимых на поверхность электрода сенсора, определяется не только разностью энергий его взаимодействия с энантиомерами, но и тем, насколько размер полости модификатора соответствует габаритам этих молекул. Открытие поможет усовершенствовать сенсорные платформы для определения химического состава лекарств в лабораториях и на производстве.
Некоторые молекулы, имея одинаковый химический состав и характер связей между атомами, существуют в двух формах, различающихся пространственным расположением атомов. По сути они представляют собой зеркальные отражения друг друга, и совместить их в пространстве невозможно, равно как правую и левую руки. Такое свойство получило название хиральность, а сами зеркальные формы молекул — энантиомеры с R- или S-конфигурацией.
В обычных условиях свойства R- и S-энантиомеров одного и того же вещества ничем не отличаются, разве что они по-разному взаимодействуют с поляризованным светом. Именно поэтому вещества, состоящие из хиральных молекул, иногда называют оптически активными. Однако в окружении других молекул с такой же особенностью, например, в живых организмах, энантиомеры могут сильно различаться по своим свойствам. Так, жаропонижающий препарат ибупрофен существует в виде двух энантиомеров, но как лекарство действует лишь один из них. В связи с этим ученым важно уметь синтезировать, разделять и идентифицировать зеркальные формы молекул, чтобы при создании современных лекарств добиваться присутствия в препарате только нужного энантиомера.
Существует довольно много способов выявить энантиомеры, однако не все из них технически доступны. Одним из наиболее простых и дешевых методов считается электрохимический анализ. В процессе измеряются ток пика и потенциал, при которых молекулы веществ вступают в электрохимическую реакцию на электроде. Энантиомеры на поверхности обычного электрода не покажут никакой разницы в токах пиков и потенциалах; если же каким-либо образом поверхности электрода придать хиральные свойства, то разница в электрохимических свойствах становится вполне регистрируемой величиной. Проще всего это сделать, нанеся на поверхность электрода модификатор — определенные хиральные молекулы или молекулярные комплексы. Главная проблема, с которой сталкиваются специалисты при разработке таких сенсоров, состоит в том, чтобы подобрать модификатор, позволяющий выявить наибольшую разницу в электрохимических свойствах энантиомеров.
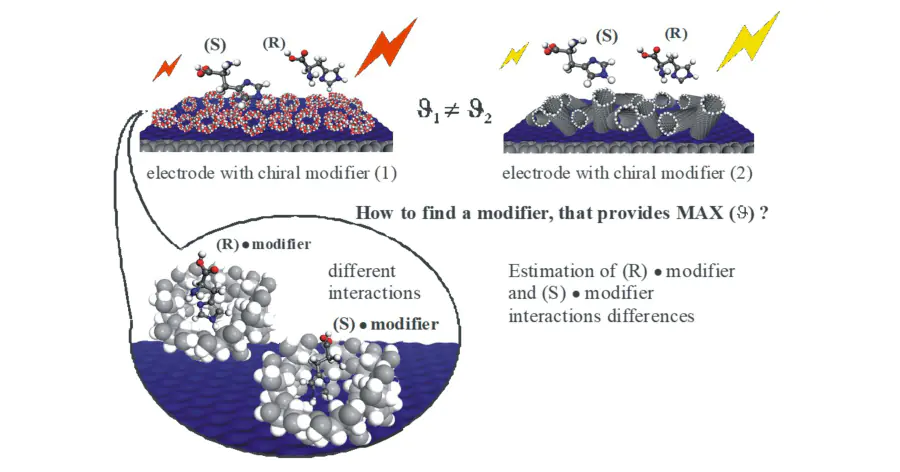
Химики из Башкирского государственного университета (Уфа) предложили теоретическую модель, с помощью которой можно определить модификатор с максимальной избирательностью. Это, в свою очередь, позволит целенаправленно создавать сенсоры с наибольшей энантиоселективностью по отношению к заданному анализируемому веществу, например, действующему компоненту лекарственного препарата. В предложенной модели эффективность хирального модификатора оценивалась по разнице энергий, необходимых для его взаимодействия с R- или S-энантиомером: чем больше была эта разность, тем большую избирательность имел модификатор.
В качестве объектов для расчетов авторы взяли два варианта хиральных модификаторов — циклодекстрины и углеродные нанотрубки. Циклодекстрины состоят из связанных между собой остатков глюкозы, а внешне напоминают усеченный конус с внутренней полостью разного размера. Углеродные нанотрубки представляют собой свернутый в полый цилиндр лист графена. Эти соединения были выбраны потому, что они уже используются в некоторых типах сенсоров для анализа, а также для хроматографического разделения энантиомеров.
Исследователи рассчитали энергию связывания энантиомеров десятка различных лекарственных препаратов и аминокислот с циклодекстринами и углеродными нанотрубками, имеющими разный диаметр полостей. Оказалось, что эффективность модификатора зависела не только от разности энергий его взаимодействия с R- и S-энантиомерами, но от того, насколько размер его полости соответствовал габаритам связываемых молекул.
«Предложенный нами алгоритм значительно упростит подбор наиболее эффективного хирального модификатора. Это поможет оптимизировать сенсорные платформы, использующиеся для установления подлинности и срока годности, а также энантиочистоты лекарственных препаратов. В дальнейшем мы планируем исследовать иные варианты хиральных модификаторов, чтобы дополнительно проверить нашу модель», — рассказывает первый автор работы Руфина Зильберг, кандидат химических наук, доцент кафедры аналитической химии Башкирского государственного университета.

