Исследователи научились контролировать концентрацию оксида азота светом
В этом им помогло новое фотоактивное соединение и система с обратной связью, которая в режиме реального времени меняет интенсивность излучения и тем самым поддерживает постоянное содержание NO. Концепция окажется полезной при разработке носимых терапевтических устройств. Результаты исследования, поддержанного грантом РНФ №18-15-00049, опубликованы в журнале Materials Today Chemistry.
Оксид азота (NO) — химически очень активная молекула, которая производится в организме человека ферментами и играет сигнальную и регуляторную функции. Из-за небольшого размера она легко проникает внутрь клеток без затрат энергии. Наиболее известная активность оксида азота — контроль за деятельностью сердечно-сосудистой системы: с его помощью происходит расслабление сосудов, снижение давления. Кроме того, NO вовлечен в другие разнообразные процессы: взаимодействие между собой нейронов мозга, цикл роста волос, поддержание иммунного ответа и прочее.
Это вещество также применяют в медицине для лечения сердечно-сосудистых заболеваний, заживления ран, активации иммунного ответа на инфекцию и при терапии рака. Однако из-за своей активности NO слишком быстро превращается в другие, уже не сигнальные молекулы, и поэтому приходится использовать соединения, которые будут его нарабатывать уже в организме пациента. И здесь возникает другая проблема — контроль за содержанием оксида азота в тканях. Например, при диабете затруднено образование новых сосудов; слишком малая концентрация NO не будет эффективна при стимуляции этого процесса, чуть большая способствует ему, а еще большая полностью подавит.
«Один из подходов — контролировать высвобождение оксида азота при, например, облучении. Особый интерес вызывают носители, способные на это под действием красного света, проникающего глубоко в ткани. Так, недавно появились сообщения о фотодонорах NO на основе ядра аза-BODIPY — популярного красителя для биологических применений, а также потенциального компонента оптоэлектроники», — рассказывает Татьяна Карогодина, кандидат химических наук, научный сотрудник лаборатории оптики и динамики биологических систем НГУ.
Именно на основе аза-BODIPY новосибирские исследователи синтезировали новое соединение AzaB-NO, выделяющее оксид азота под действием ближнего инфракрасного света. Количество NO зависит от интенсивности излучения, что позволяет достаточно точно настраивать его концентрацию. Максимально она может быть вдвое выше концентрации изначально введенного фотодонора, поскольку каждая молекула последнего теоретически выделяет две молекулы оксида. В отсутствие света вещество присоединяет NO обратно, а значит, может работать как своего рода буферная система.
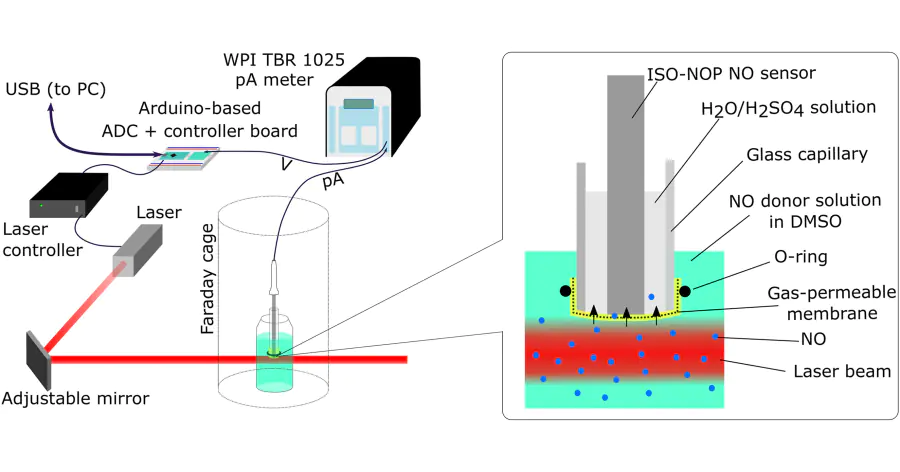
Также авторы реализовали систему с обратной связью, которая активно поддерживает заданную концентрацию NO в образце, управляя интенсивностью лазерного излучения. Она состоит из датчика для определения содержания оксида в растворе в режиме реального времени и специального отсека, который содержит фотодонор и освещается светом. Тут ученые столкнулись с проблемой: AzaB-NO не растворяется в воде — только в органике, но ее воздействие может вывести сенсор из строя. Тогда они просто разделили их обычным парафильмом, выполняющим роль мембраны. Он не пропускает жидкость, но все еще проницаем для маленького NO.
«Эта до смешного простая и доступная идея — не просто техническое решение, но целая концепция того, как использовать нашу систему в биомедицине. Раствор фотодонора можно поместить в аналогичную газопроницаемую мембрану (например, капсулу) и ввести в организм: в результате к тканям проникнет только необходимый оксид азота, но не потенциально токсичные побочные продукты», — объясняет Александр Москаленский, кандидат физико-математических наук, заведующий лабораторией оптики и динамики биологических систем НГУ.
Разработка может стать основой носимых и имплантируемых устройств для терапии раковых, сердечно-сосудистых и метаболических заболеваний, однако еще предстоит проверить ее на клетках и животных.

