Наносеребро помогло изучить конформации важнейшего белка «энергостанций» клеток
Митохондрии — своего рода «энергетические станции» клеток, которые окисляют органические соединения для получения энергии. Она идет на синтез единой «энерговалюты» АТФ, выделение тепла и поддержание жизненно важного электрохимического потенциала. Происходит это в результате работы электрон-транспортной (дыхательной) цепи, один из основных участников которой — небольшой белок цитохром с. Обычное его месторасположение — в межмембранном пространстве митохондрий, однако он может выходить из органеллы в цитоплазму и запускать программируемую клеточную гибель.
Сбои в работе митохондрий могут стать причиной большого количества патологий, например, нарушений работы нервной и сердечно-сосудистой систем, метаболических и онкологических заболеваний. Конформация и, соответственно, активность цитохрома с при этом изменяется, однако до сих пор не было способа, который позволил бы отследить эти процессы в нетронутой митохондрии и без выделения белка.
Группа российских ученых с зарубежными коллегами разработала новый подход на основе метода спектроскопии гигантского комбинационного рассеяния (ГКР) для изучения цитохрома с в митохондриях. Этот метод — улучшенная версия рамановской спектроскопии, уже применявшейся при исследовании цитохромов, однако неспособной различить слабый сигнал от разных конформаций белка, которые он может принимать при изменении условий. Ранее авторы уже выяснили, что наноструктурированная серебряная подложка способна усилить этот сигнал при проведении ГКР. Теперь же они впервые представили его как высокочувствительный и селективный инструмент для изучения конформационных изменений гема (комплексного соединения железа) в окисленном цитохроме с в неповрежденных функционирующих митохондриях и для оценки скорости транспорта электронов в дыхательной цепи.
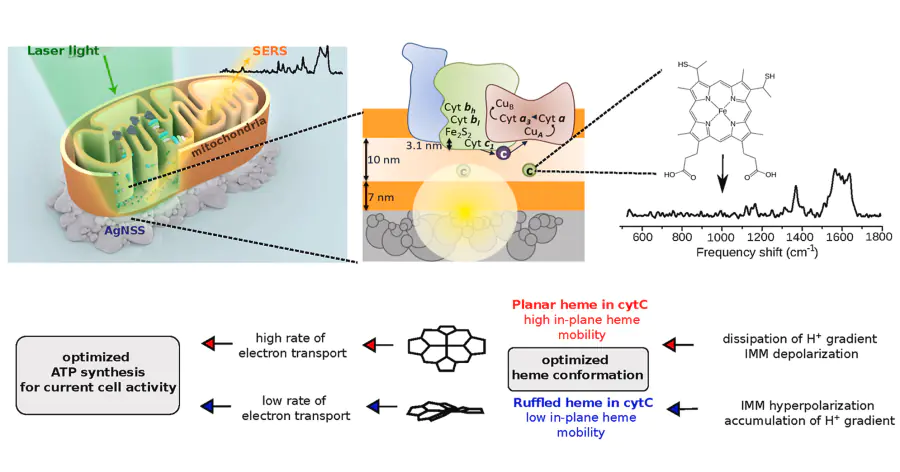
Сергей Новиков, старший научный сотрудник лаборатории контролируемых оптических наноструктур МФТИ, рассказывает: «Гигантское комбинационное рассеяние имеет максимальный сигнал, когда наночастицы контактируют с молекулами. Чем дальше находится молекула от частицы, тем сигнал слабее. Интересующий нас белок цитохром с находится в межмембранном пространстве митохондрий, на расстоянии 7–12 нанометров от внешней мембраны. На обычной плоской серебряной подложке мы можем видеть ГКР-сигнал в основном от компонентов внешней митохондриальной мембраны. В случае специфической конфигурации серебрянной наноструктурированной поверхности, разработанной коллегами с ФНМ МГУ и предложенной в нашей работе, мы смогли увидеть, что происходит с цитохромом с в межмембранном пространстве митохондрий. За счет высокой чувствительности метода мы видим даже изменения, которые произошли только в небольшом количестве белков цитохрома с. Эти изменения могут быть связаны с зарождающейся патологией. То есть, когда клетка в целом еще здоровая, мы можем отследить зарождение патологии на ранней стадии по изменениям в этих белках».
Ученые постепенно усложняли исследуемый объект от модельных до реальных митохондрий. Анализировался сигнал SERS от этих объектов, нанесенных на подложку c наночастицами серебра. С помощью сканирующей и просвечивающей электронной микроскопии и теоретического моделирования физикам удалось построить распределение электрических полей для подложки с исследуемым объектом и объяснить, почему усиливается сигнал именно от цитохрома с: в полученной конфигурации подложки и объекта белок оказывается в «зоне видимости» ГКР.
«Нужно было проверить, что митохондрии не изменяют свое состояние, когда контактируют с серебряными структурами, что серебряные структуры не изменяют своих свойств, что получаемый сигнал ГКР обладает высокой воспроизводимостью. Надо было на разных системах доказать, что спектр ГКР, регистрируемый от митохондрий, связан с определенными колебаниями атомов именно в цитохроме с, а не в других белках митохондрий, и показать, что наблюдаемые спектры отражают работу дыхательной цепи. У нас это все получилось», — комментирует Надежда Браже, ведущий научный сотрудник лаборатории общей биофизики биологического факультета МГУ.
В результате ученые получили метод наблюдения за белками внутри клеток, который может стать основой для создания сенсоров для диагностики заболеваний на ранних стадиях.