МикроРНК в везикулах стволовых клеток помогли разрешить фиброз легких
Тяжелая и хроническая пневмония развивается в результате легочных инфекций, среди которых и COVID-19, а также аутоиммунных заболеваний, ожогов, воздействия токсикантов и прочего. При этом воспаляется ткань, через которую происходит газообмен, и затем возможно ее замещение на нефункциональную соединительную — возникают так называемые фибротические очаги. Последние составляют преимущественно миофибробласты, в чрезмерных количествах синтезирующие коллаген и способные к сокращению за счет волокон гладкомышечного актина. К краям таких очагов подтягиваются новые фибробласты (которые могут дифференцироваться в миофибробласты), расширяя площадь пораженных областей и вызывая их слияние. Здоровой ткани становится все меньше, и дыхательная функция легких драматически ухудшается.
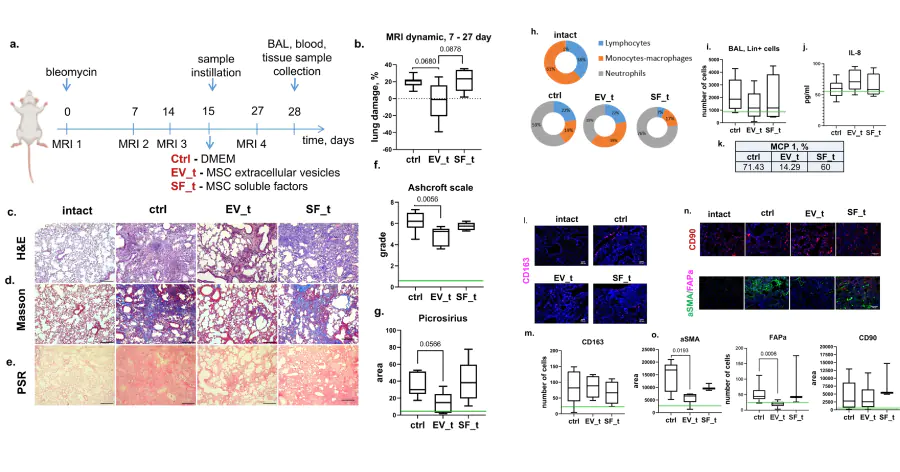
Один из наиболее многообещающих подходов к лечению фиброзов связан с использованием мезенхимальных стволовых клеток (МСК), а точнее секретируемых ими молекул. Они могут способствовать разрушению патологического внеклеточного матрикса и воздействовать на активность и судьбу окружающих клеток. В своем новом исследовании сотрудники Медицинского научно-образовательного центра МГУ имени М.В. Ломоносова и Научно-исследовательского института морфологии человека имени академика А.П. Авцына оценили, как влияют разные секреты МСК на развитие и разрешение фиброза легких у мышей, вызванного воздействием блеомицина — цитатостатика, который применяют при лечении некоторых видов рака. В рамках терапии они однократно (спустя две недели после запуска патологии или же перед ним) впрыскивали в трахею животных жидкость, содержащую выделяемые МСК сигнальные молекулы — факторы роста — или везикулы с микроРНК, не кодирующими белки, но выполняющими регуляторные задачи.
Профилактическое лечение перед воздействием блеомицина не смогло предотвратить образование фиброзных очагов. Авторы считают, что подобная терапия может быть успешной, если проводить ее в другое время, в некую «активную фазу», когда легкие непосредственно повреждаются. Идею подтверждают эксперименты их коллег, которые вводили цитостатик и везикулы совместно.
Вместе с тем, лечение уже развившегося фиброза оказалось очень действенным в случае везикул с микроРНК — постепенно состояние легких больных мышей стало сравнимо с таковым у здоровых животных. Ученые наблюдали уменьшение количества миофибробластов — главных «виновников» патологического состояния. Причиной стало истощение пула именно клеток-предшественников, то есть проблема решалась на корню. Доказательством того, что именно микроРНК регулируют активность нежелательной популяции, стали эксперименты, когда в терапевтическую субстанцию добавляли ферменты, расщепляющие рибонуклеиновую кислоту: тогда препарат просто переставал работать.
Ученые смогли выяснить и то, какие конкретно молекулы РНК оказывают эффект. Избирательно подавляя активность разных их сортов, авторы нашли необходимые — miR-21, которые уже известны своей способностью регулировать фибротические процессы, а также miR-29c и miR-129. Как действуют две последних молекулы, до конца неясно. С одной стороны, они могут ослаблять чрезмерно активные и устойчивые к апоптозу миофибробласты. С другой стороны, эти микроРНК, вероятно, влияют на дифференцировку фибробластов в миофибробласты, предотвращая ее, и возвращают миофибробласты в состояние предшественников, а еще опосредованно модулируют структуру и состав внеклеточного матрикса. В совокупности это способствует разрешению фибротических очагов.
Таким образом, авторы продемонстрировали эффективность нового подхода к лечению тяжелых последствий пневмонии. Вместе с тем, перед внедрением подхода в медицинскую практику еще предстоит ответить на ряд вопросов, например, как именно производить препарат, каков точный механизм его работы и какой режим лечения будет наиболее действенным и комфортным для пациента.



