Российские ученые придумали, как сделать лучевую терапию рака безопаснее
К наиболее эффективным методам лечения злокачественных опухолей относится радионуклидная лучевая терапия. При таком воздействии новообразование разрушается благодаря тому, что пациенту в кровь вводят радионуклиды — нестабильные атомы, которые, распадаясь, испускают ионизирующее излучение. Российские ученые разработали систему доставки, которая поможет минимизировать воздействие радиации на здоровые ткани и уберечь их от разрушения. Результаты исследования, поддержанного грантом Российского научного фонда (РНФ), опубликованы в журнале Journal of Colloid and Interface Science.
По данным Международного агентства по изучению рака (IARC), ежегодно в мире регистрируется более двенадцати миллионов новых случаев онкологических заболеваний и около шести миллионов смертей от них.
На сегодняшний день существует три основных способа лечения опухолей: химиотерапия, хирургическое удаление и лучевая терапия. Первые два метода не всегда эффективны, поскольку раковые клетки со временем приобретают устойчивость к лекарственным препаратам, а все распространившиеся по организму метастазы бывает невозможно выявить и удалить. Третий метод убивает опухоли безотказно: к ионизирующему излучению невозможно приобрести устойчивость. В ходе лечения пациенту в кровь вводят радионуклиды — нестабильные атомы, ядра которых распадаются и образуют ионизирующие частицы. Они несут большое количество энергии, которая повреждает клетки опухоли: разрушает их мембрану, ДНК, изменяет протекающие внутри них биохимические реакции. С помощью специальных молекулярных «меток» радионуклиды распознают только раковые клетки и накапливаются в месте возникновения опухоли.
Существенный недостаток описанного подхода заключается в том, что до тех пор, пока радиоактивный изотоп не достигнет опухоли, он будет повреждать здоровые ткани организма из-за испускания ионизирующего излучения при радиоактивном распаде. Поэтому ученые разрабатывают специальные носители, которые помогают «удержать» радионуклид и его дочерние изотопы — атомы, на которые он распадается, — до момента их доставки к раковым клеткам. Для этого используются пептиды (короткие молекулы белков), искусственные мембранные пузырьки, а также наночастицы из неорганических соединений. Но лучшие из них удерживают максимум 84% радионуклидов, а остальные 16% все также поражают здоровые ткани.
Исследовательская группа из Российского научного центра радиологии и хирургических технологий имени академика А. М. Гранова (Санкт-Петербург), Санкт-Петербургского политехнического университета Петра Великого (Санкт-Петербург), Национального исследовательского университета ИТМО (Санкт-Петербурга) и Национального исследовательского Томского политехнического университета (Томск) разработала систему доставки радионуклида актиния-225 (225Ac), которая удерживает более 98% этих изотопов внутри своей структуры. Ученые выбрали в качестве терапевтического агента радионуклид 225Ac, так как при его радиоактивном распаде образуется четыре альфа-частицы с большим количеством энергии, достаточной для эффективного разрушительного воздействия на опухоль. Кроме того, этот изотоп, в отличие от других, обладает относительно длинным периодом полураспада, то есть временем, в течение которого его активность снизится в два раза. Период полураспада 225Ac равен десяти суткам, что дает преимущество при его производстве, хранении и транспортировке в медицинские центры.
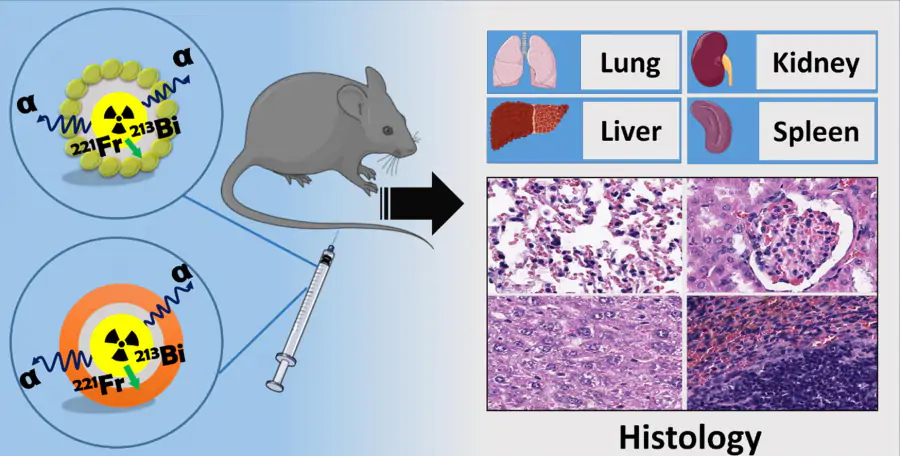
В качестве носителей радионуклида 225Ac ученые разработали и синтезировали наночастицы, состоящие из диоксида кремния. Затем к наночастицам химически присоединили радионуклиды и сверху покрыли пленкой из золота или титансодержащего органического соединения. Именно эти дополнительные слои должны были предотвратить отсоединение 225Ac от частиц-носителей и его хаотичное циркулирование по организму, приводящее к повреждению здоровых тканей и органов.
Чтобы проверить, действительно ли наночастицы способны удержать радионуклид, биологи ввели образцы в виде суспензии в хвостовую вену мышей. На первый, третий и десятый день после терапии животных безболезненно умерщвляли, а их органы исследовали на радиоактивность, которая была признаком распада 225Ac. В качестве группы контроля исследователи использовали мышей, которым вводили чистый 225Ac без наночастиц-носителей или с наночастицами, но без покрытия из золота или титана.
Оказалось, что во всех контрольных вариантах уже на третий день радионуклид накапливался в печени, селезенке и легких, приводя к отмиранию клеток этих органов. Напротив, наночастицы с 225Ac, дополнительно покрытые слоем золота или титана, практически не вредили здоровым тканям даже через десять суток.
«Наша разработка позволит безопасно доставлять радионуклиды к опухолям, не нанося вреда здоровым тканям организма. Помимо опытов на животных, мы провели исследования in vitro — "в пробирке", — которые доказали, что синтезированные нами частицы удерживают 225Ac в стабильном состоянии на протяжении тридцати дней. Следующий этап исследования — модификация поверхности наночастиц с помощью особых молекулярных "меток", которые позволят разработанным нами компонентам направленно мигрировать к раковым клеткам, и тем самым обеспечат избирательность терапии», — рассказывает Тимофей Карпов, сотрудник группы нанофармакологии лаборатории генной инженерии Российского научного центра радиологии и хирургических технологий имени академика А. М. Гранова.

