Ученые предложили «обратную» стратегию образования С-О связи
Нуклеофильное замещение при атоме углерода — это фундаментальное органическое превращение. В его хрестоматийной версии нуклеофильный реагент замещает связанный с углеродом атом или хорошо уходящую группу атомов. Нуклеофильное замещение при электрофильном атоме углерода кислородным нуклеофилом является самой широко используемой стратегией для создания связей С-О.
В отличие от этого, нуклеофильное замещение при атоме кислорода встречается гораздо реже, поскольку связи O-X обычно неблагоприятно поляризованы, и богатые электронами атомы кислорода являются плохими мишенями для нуклеофилов. Поэтому «обращенные» подходы, когда углерод-центрированный нуклеофил реагирует с кислородным электрофилом, относительно мало распространены.
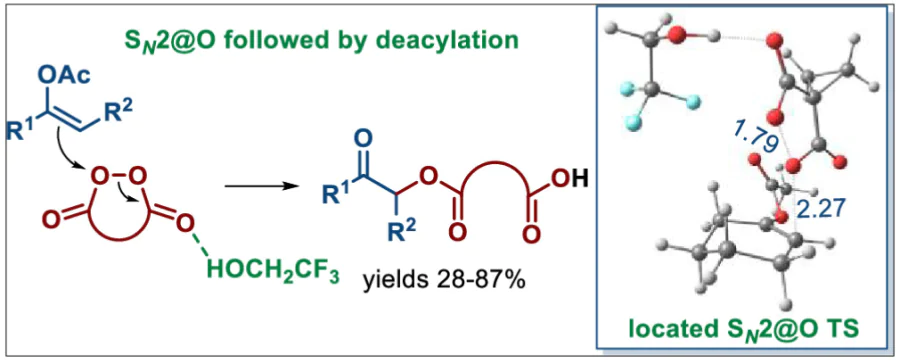
Ученые ИОХ РАН совместно с коллегами из Университета штата Флорида предложили неожиданную альтернативу общепринятым подходам к созданию С-О связей — взаимодействие O-электрофилов, таких как органические пероксиды, с углеродными нуклеофилами. Было обнаружено, что нуклеофильное замещение при атоме кислорода циклических диацилпероксидов электронно-насыщенным атомом углерода енолацетатов с последующим деацилированием приводит к α-ацилоксикетонам с дополнительной карбоксильной группой. Анализ процесса квантово-химическими методами показал, что ключевая стадия протекает как бимолекулярная нуклеофильная реакция замещения (SN2) при атоме кислорода (SN2@O). Используемый растворитель CF3CH2OH играет двойную роль, помогая на обоих этапах реакционного каскада: он снижает энергию активации SN2@O за счет образования водородной связи с отдаленным карбонилом и способствует деацилированию промежуточного катионного интермедиата.
Работа опубликована в The Journal of Organic Chemistry (IF = 4.20)
Профили учёных из новости
Лаборатории из новости
Группа теоретической химии ИОХ РАН

Междисциплинарная лаборатория мирового уровня «Редокс-активных молекулярных систем»