Ферменты бактериофагов помогут победить внутрибольничные инфекции
Бактерии быстро приобретают устойчивость к антибиотикам и передают это свойство друг другу, что особенно часто происходит в больничных условиях. Разрыв между изобретением нового антибиотика и формированием резистентных к нему штаммов постоянно сокращается, в связи с чем проблема антибиотикоустойчивости стоит в настоящее время чрезвычайно остро. Ученые ФИЦ Биотехнологии РАН вместе с коллегами из ИБХ РАН и других российских институтов детально исследовали ферменты-деполимеразы из ряда бактериофагов — вирусов, паразитирующих на высокопатогенной бактерии Acinetobacter baumannii, которая вызывает пневмонию, урологические инфекции, менингит и другие тяжелые осложнения. Использование данных ферментов, способствующих разрушению клеточной стенки бактерии, является перспективной альтернативой антибиотикотерапии.
Бактерия Acinetobacter baumannii, получившая название в честь американских бактериологов Пола и Линды Бауманн, вызывает опасную внутрибольничную инфекцию и внесена Всемирной организацией здравоохранения в список приоритетных патогенов для разработки антибактериальных агентов. Одной из перспективных альтернатив классической антибиотикотерапии является использование бактериофагов или коктейлей из их отдельных ферментов, разрушающих бактерии. Ученые из ФИЦ Биотехнологии РАН вместе с коллегами из Москвы и Оболенска исследовали ферменты-деполимеразы ряда бактериофагов из рода Friunavirus, паразитирующих на различных штаммах бактерий Acinetobacter baumannii.
«Всемирная организация здравоохранения уже около 10 лет назад заявила, что мы вошли в постантибиотиковую эпоху. Нередко бактерии вырабатывают устойчивость еще до того, как антибиотик выпущен на рынок. Именно поэтому так важно искать новые способы борьбы с патогенными микроорганизмами. Мои коллеги работают с естественными врагами Acinetobacter baumannii — бактериофагами из рода Friunavirus», — рассказывает старший научный сотрудник лаборатории инженерной энзимологии ФИЦ Биотехнологии РАН, к.б.н. Константин Бойко.
Эти бактериальные вирусы узнают патогенную бактерию-хозяина благодаря ферментам под названием TSD (аббревиатура для tailspike depolymerase, буквально — «деполимераза хвостового шипа»). Такие ферменты разрезают разветвленные молекулы полисахаридов, находящиеся во внешней оболочке бактерии и служащие ей естественной защитой, тем самым способствуя гибели клетки. Важно отметить, что в отличие от антибиотиков, которые «не разбираются» между вредными и полезными бактериями и, в частности, требуют восстановления микрофлоры после приема, фаговые деполимеразы чрезвычайно специфичны по отношению к бактерии-патогену, тем самым обеспечивая безопасность для других клеток, находящихся рядом.
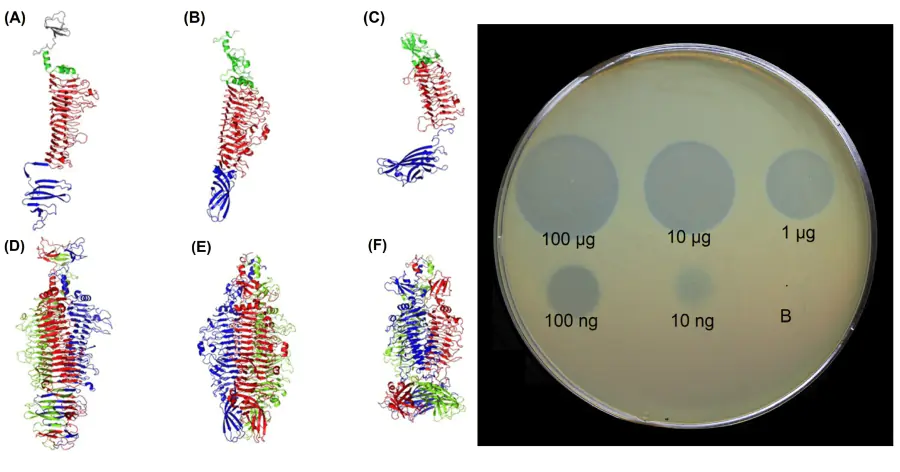
«В нашей совместной работе мы идентифицировали и комплексно исследовали ряд таких деполимераз, специфичных к серьезному патогену — Acinetobacter baumannii. В частности, методом рентгеноструктурного анализа нами была установлена пространственная структура этих ферментов», — поясняет Константин Бойко.
Чтобы показать потенциальную антимикробную активность фаговых деполимераз, модельный организм — личинок восковой моли — заразили штаммом Acinetobacter baumannii K9, что, предсказуемо, привело к их высокой смертности. При этом наличие в среде одного из исследованных ферментов существенно снижало летальность. Полученные результаты демонстрируют, что деполимеразы бактериофагов являются перспективным объектом для борьбы с различными патогенами, в том числе обладающими множественной лекарственной устойчивостью.




