Ученые продемонстрировали увеличение внутриопухолевого накопления и усиление противоопухолевого эффекта, используя стратегию двойного нацеливания
Традиционная адресная доставка химиотерапевтических и диагностических агентов с использованием наноносителей является многообещающим подходом для тераностики рака. К сожалению, этот подход часто сталкивается с затрудненным доступом к опухоли, что снижает терапевтический индекс и ограничивает дальнейшую клиническую трансляцию разрабатываемого препарата. Используя стратегию двойного нацеливания, ученые продемонстрировали увеличение внутриопухолевого накопления и заметное усиление противоопухолевого эффекта, что привело к синергизму высокого уровня по сравнению с монотаргетными конъюгатами.
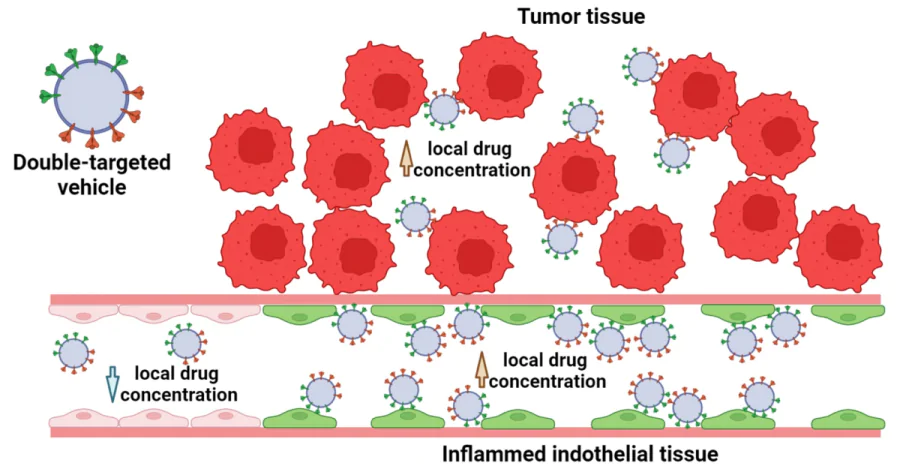
Ученые Лаборатории биотехнологий и наноструктур для адресной доставки лекарств и Лаборатории Магнитной томографии и спектроскопии продемонстрировали стратегию одновременного двойного нацеливания на два разных участка опухолевой ткани: опухолевый эндотелий и рецепторы клеточной поверхности, для проведения тераностики онкологических заболеваний наноразмерными системами доставки препаратов адресного действия
В качестве системы доставки были использованы полиамидаминовые дендримеры четвертого поколения (G4), модифицированные Gd - DTPA. В качестве мишеней были выбраны Р-селектин, маркер воспаленной сосудистой сети, также характерный для опухолевой ткани, и рецептор альфа-фетопротеина человека (АФПР), являющийся маркером широкого спектра опухолей, в том числе присутствующий и на клетках SKOV-3.
Дендримеры были функционализированны пептидом, обладающим сродством к селектину (что будет способствовать захвату конъюгата в воспалительном микроокружении опухоли и усилит экстравазацию), и пептидом к АФПР (что позволит увеличить накопление препарата в опухолевых клетках). Полученный конъюгат с двумя векторными молекулами (G4-DTPA-PEG-Pep) продемонстрировал высокие уровни интернализации клетками SKOV-3. In vitro оценка релаксации r1 и r2 G4-DTPA-PEG-Pep выявила значения, сходные со значениями коммерчески доступного препарата Magnevist.
В эксперименте in vivo G4-DTPA-PEG-Pep продемонстрировал незначительно более низкую МРТ-контрастирующую способность по сравнению с Magnevist, а при изучении более длительных периодов накопления, Cy5.5-меченый G4-DTPA-PEG-Pep, демонстрировал четкую локализацию в опухолевых клетках и тканях in vivo. Также было показано увеличение противоопухолевого эффекта по сравнению с монотаргетными конъюгатами.
Таким образом, предложенная стратегия, использующая двойное нацеливание на опухолевые ткани, может способствовать увеличению накопления лекарственных препаратов в раковых клетках как для терапевтических, так и для диагностических целей.
Профили учёных из новости
Лаборатории из новости
Лаборатория биотехнологий и наноструктур для адресной доставки лекарств

Лаборатория Магнитной томографии и спектроскопии